Kỹ Thuật Nuôi, Tin tức
Hiệu Ứng Tích Lũy Và Điều Hòa Từ Hỗn Hợp Kim Loại Zn, Pb Và Cd Trong Tôm Nhiệt Đới Penaeus vannamei
Tóm tắt
Ô nhiễm kim loại nặng đang trở thành một mối đe dọa nghiêm trọng đối với môi trường, đặc biệt là các hệ sinh thái thủy sinh nhạy cảm như vùng cửa sông và đầm phá ven biển. Việc hiểu rõ tác động của kim loại nặng lên sinh vật sống trong các khu vực này là yếu tố then chốt để đưa ra giải pháp bảo vệ và duy trì cân bằng sinh thái. Nghiên cứu này tập trung đánh giá khả năng điều hòa kim loại của tôm thẻ chân trắng (Penaeus vannamei) – một loài thủy sản có giá trị kinh tế cao và phổ biến tại vùng cửa sông. Ba kim loại nặng thường gặp gồm kẽm (Zn), chì (Pb) và cadmium (Cd) được xem xét cả riêng lẻ và trong điều kiện kết hợp, nhằm làm rõ cơ chế tương tác và ảnh hưởng của chúng. Kết quả cho thấy, tôm con có thể tự điều chỉnh hàm lượng kẽm và chì trong cơ thể, song cadmium lại có xu hướng tích lũy mà không được bài tiết ở nồng độ thử nghiệm. Điều này cho thấy trong môi trường cửa sông, tôm thẻ chân trắng có thể đóng vai trò như một sinh vật chỉ thị sinh học hiệu quả đối với cadmium, góp phần quan trọng trong việc giám sát và đánh giá mức độ ô nhiễm kim loại nặng.
Giới thiệu
Nuôi tôm he thâm canh, bao gồm cả tôm thẻ chân trắng (Penaeus vannamei), là một ngành kinh tế quan trọng của Mexico, chủ yếu phát triển tại các cửa sông và vùng ven biển Thái Bình Dương. Tuy nhiên, môi trường nuôi tôm tại đây thường chứa hỗn hợp nhiều kim loại nặng như niken (Ni), kẽm (Zn), chì (Pb), cadimi (Cd) cùng các nguyên tố khác, có thể gây ảnh hưởng tiêu cực đến hệ sinh vật thủy sinh, bao gồm cả tôm nuôi. Mặc dù nồng độ kim loại hòa tan trong nước thường không đủ cao để gây chết trực tiếp, nhưng chúng có thể tích lũy dần trong cơ thể tôm, dẫn đến tác động mãn tính. Nhiều nghiên cứu đã chỉ ra rằng, sự tích tụ kim loại ở tôm thẻ giai đoạn post-larvae có thể làm thay đổi quá trình hô hấp, bài tiết amoniac, điều hòa thẩm thấu, khả năng ăn và hấp thu dinh dưỡng. Tôm hấp thụ kim loại qua mang và bề mặt cơ thể (thông qua quá trình hấp phụ hoặc hấp thu), cũng như qua đường tiêu hóa khi ăn thức ăn hoặc lọc nước. Ngược lại, kim loại có thể được bài tiết hoặc lưu trữ tạm thời tại các cơ quan như gan tụy, gan, thận hoặc tuyến râu. Nếu quá trình bài tiết diễn ra hiệu quả, tôm vẫn có thể duy trì trạng thái khỏe mạnh. Tuy nhiên, khi nồng độ kim loại vượt quá khả năng điều tiết của cơ thể, tôm sẽ gặp rối loạn sinh lý, thậm chí dẫn đến tử vong. Mức độ ảnh hưởng của kim loại nặng phụ thuộc vào nhiều yếu tố, bao gồm mức độ ô nhiễm môi trường, loài và giai đoạn phát triển của tôm, loại kim loại gây ô nhiễm, cũng như điều kiện môi trường sống.
Kim loại độc hại, dù không gây chết ngay lập tức, vẫn có thể gây ra những thay đổi tiêu cực cho nhiều loài sinh vật, bao gồm tôm thẻ chân trắng (Penaeus vannamei). Những thay đổi về hình thái hoặc mô học chẳng hạn như biểu mô mang dày lên, mẫu hemolymp thay đổi, làm giảm khoảng trống và làm giảm lưu lượng máu trong mang. Tác động dưới mức gây chết cũng có thể bao gồm những thay đổi về sinh lý, ảnh hưởng đến sự tăng trưởng, phát triển, khả năng bơi lội, sinh hóa tế bào, hoạt động enzyme, nội tiết, hành vi và sinh sản. Hiểu rõ cách tôm thẻ chân trắng tích lũy và điều hòa kim loại độc hại rất quan trọng do chúng đóng vai trò quan trọng trong môi trường và nền kinh tế và có thể được sử dụng như sinh vật chỉ thị để theo dõi ô nhiễm kim loại. Nghiên cứu này tập trng vào khả năng tích lũy và loại bỏ kim loại của tôm thẻ chân trắng P. vannamei ở giai đoạn non và tiềm năng của nó như một loài chỉ thị về ô nhiễm kim loại, khả năng chịu đựng hoặc độ nhạy cảm với một số mức kim loại nhất định được báo cáo ở vùng ven biển Mexico.
Vật liệu và phương pháp
Mẫu tôm
Nghiên cứu sử dụng cá thể tôm thẻ chân trắng (P. vannamei) non với tổng chiều dài khoảng 1 cm. Tôm được lấy từ Cultivos Acuícolas Aquapacific S.A. de C.V. ở Mazatlán, Sinaloa, Mexico và thích nghi trong 2 tuần. Tôm được nuôi trong nước biển nhân tạo (Instant Ocean®) ở 25 (psu), chu kỳ ngày-đêm12–12 giờ, pH 8,1, và 25°C. Nước biển nhân tạo mang lại sự ổn định hóa lý cho các môi trường thử nghiệm và hỗ trợ quá trình hấp thụ vi lượng kim loại hiệu quả. Tôm được cho ăn bằng hai loại protein cá (Sure Start Larval Diet 3–4 và Sanoquart®), ba lần một ngày để đạt kích cỡ tổng chiều dài từ 1,0 đến 3,5 cm.
Thiết kế thử nghiệm
Nồng độ kim loại hòa tan sử dụng trong thí nghiệm mô phỏng thực tế ô nhiễm kim loại ở các bờ biển Mexico. Tôm được thả riêng lẻ và cho ăn 2 ngày một lần trong 1 giờ; sau đó, nước được thay để giữ chất lượng nước và nồng độ oxy hòa tan thích hợp. Các độ pha loãng Zn, Pb và Cd (Tiêu chuẩn độ tinh khiết cao®) được áp dụng trong một thí nghiệm lần lượt (kim loại với kim loại) và thí nghiệm kết hợp (hỗn hợp của ba kim loại). Nồng độ được kiểm tra là 87,21 μg/l Cd, 191,16 μg/l Pb và 9,29 μg/l Zn ở 25 psu, 25°C, pH8,1, OD ≥5,0; NH4 0,2 và NO 5,0.
Nghiên cứu tiềm năng tích lũy và điều hòa
Các thiết kế thí nghiệm bao gồm 10 nhóm thí nghiệm riêng biệt, mỗi nhóm có 10 con tôm. 20 con đối chứng (không phơi nhiễm kim loại) và 80 con phơi nhiễm với kim loại. 2 nhóm được sử dụng cho mỗi nghiệm thức (một nhóm đối chứng và một nhóm phơi nhiễm). Sau 10 ngày phơi nhiễm, tôm được giết ở nhiệt độ 2–3°C, đồng thời đo trọng lượng và tổng chiều dài của chúng (từ đầu đến đuôi). Các mẫu toàn thân được sấy khô trong 2 ngày ở 60°C và sau đó được phân hủy để phân tích hóa học như mô tả dưới đây. Đối với thí nghiệm về khả năng điều hòa kim loại, hai nhóm tôm con khác (tương ứng là đối chứng và phơi nhiễm với kim loại) được nuôi thêm 10 ngày trong nước biển nhân tạo không chứa kim loại. Ghi nhận tỷ lệ sống của tôm con trong tất cả các điều kiện thí nghiệm. Mỗi con tôm con được phân tích riêng lẻ.
Phân tích kim loại
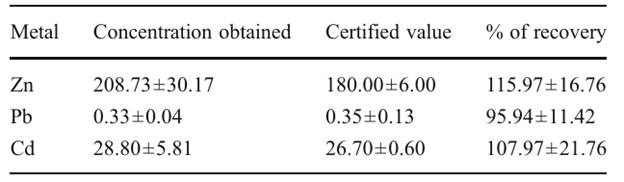
Các mẫu được phân hủy (100°C, 1 giờ) bằng axit nitric siêu tinh khiết (HNO3, Thuốc thử siêu tinh khiết Ultrex II, J.T. Baker®). Sau khi tiêu hóa, nồng độ kim loại được xác định sau khi pha loãng với nước khử ion bằng ICP-MS (Agilent 7500ce), sử dụng indium và rhenium làm chất chuẩn nội. Các phương pháp phân tích được xác nhận bằng hiệu chuẩn xen kẽ bên ngoài và bằng cách sử dụng nguyên liệu tham khảo tiêu chuẩn gan tụy tôm hùm (TORT-2, Hội đồng Nghiên cứu Quốc gia, Canada) với hiệu suất thu hồi trên 95 % (Bảng 1). Kết quả được biểu thị bằng microgam trên gam trọng lượng khô.
Phân tích thống kê
Theo Fowler và cộng sự, tất cả dữ liệu liên quan đến nồng độ kim loại và các giá trị hình thái của kích thước, trọng lượng và giá trị nồng độ độ lệch chuẩn trung bình (SD) đều được phân tích theo phân bố chuẩn và thống kê, bằng các quy trình tham số bao gồm phân tích đơn biến và phân tích đồng nhất cho các mẫu nhỏ. Phân tích Student t-test (p<0,05) được thực hiện để so sánh nồng độ kim loại và được thực hiện trong STATISTICA 5.1 dành cho Windows (StatSoft Inc.).
Kết quả và thảo luận
Nồng độ kim loại được phát hiện trong tôm P. vannamei được thể hiện trong Bảng 2. Kẽm (Zn) được tìm thấy ở tất cả các nhóm, bao gồm cả nhóm đối chứng (Hình 1; >60 μg/g). Zn là kim loại có hàm lượng cao nhất (hơn 60 μg/g) do vai trò quan trọng trong các chức năng sinh học của tôm. Nồng độ Zn trong cơ thể tôm được điều trị bằng Zn không tăng đáng kể so với nhóm đối chứng, cho thấy khả năng điều hòa Zn của tôm. Tuy nhiên, các nhóm tiếp xúc với Zn cùng với hai kim loại khác (Zn-Mx) có tổng nồng độ Zn cuối cùng cao hơn đáng kể (Bảng 2), cho thấy sự tích lũy Zn sau 10 ngày phơi nhiễm. Nồng độ Zn lần lượt là 61,64±51,03 μg/g trong đối chứng (CTL), 114,12±44,14 μg/g trong nhóm Zn và 304,42±63,65 μg/g trong Zn-Mx. Kết quả này cho thấy hỗn hợp kim loại có thể làm tăng gấp 5 lần sự hấp thu ion Zn từ môi trường. Hình 1 cho thấy sự thay đổi nồng đọ Zn trong cơ thể tôm theo thời gian. Nồng độ Zn ổn định và thậm chí giảm nhẹ sau 10 ngày làm sạch (hình 2, ngày 20). Nồng độ Zn không có sự khác biệt giữa nhóm đối chứng và nhóm thử nghiệm sau 10 ngày phơi nhiễm (Hình 2; Bảng 3). Nồng độ Zn giảm nhẹ được quan sát thấy vào ngày 20 (Hình 2) nằm trong phạm vi bình thường. Nhiều nghiên cứu đã chứng minh khả năng điều hòa Zn của các loài thủy sinh khác nhau, bao gồm cả tôm thẻ chân trắng (Litopenaeus vannamei). Tôm thẻ chân trắng có thể điều chỉnh mức độ phơi nhiễm Zn cụ thể lên tới 0,2 mg/l. Tuy nhiên, trong thí nghiệm này, sự gia tăng lượng Zn trong cơ thể được quan sát thấy ở những sinh vật được xử lý bằng hỗn hợp kim loại (Hình 1). Lượng Zn tăng có thể do sự tương tác giữa các kim loại, thay đổi cấu trúc cơ thể, hạn chế khả năng điều hòa. Tuy nhiên, khả năng điều hòa Zn của tôm có thể vẫn duy trì sau khi phơi nhiễm kim loại, cho phép tôm ổn định nồng độ Zn trong cơ thể (Hình 2). Các quan sát này phù hợp với kết quả nghiên cứu trước đây về khả năng điều hòa kim loại của các loài giáp xác khác.
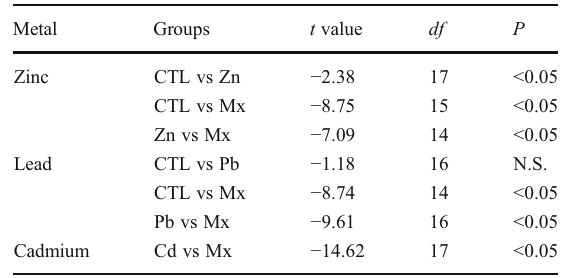
Việc so sánh được thực hiện giữa nhóm đối chứng và nhóm hỗn hợp được xử lý kim loại và/hoặc nhóm hỗn hợp kim loại
CTL: đối chứng, hỗn hợp kim loại Mx, N.S. không khác biệt đáng kể
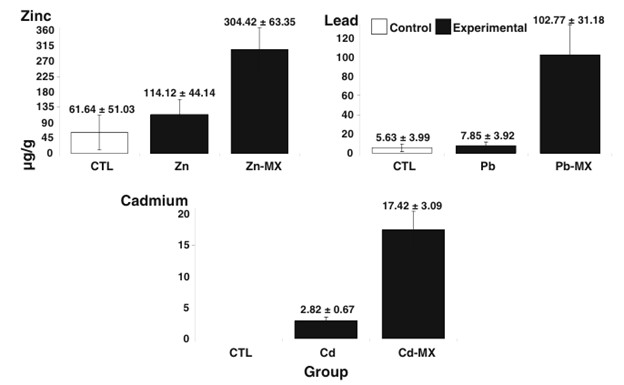
Tôm thẻ chân trắng (P. vannamei) có khả năng điều hòa chì trong cơ thể khi tiếp xúc với kim loại này đơn lẻ. Nồng độ chì trung bình trong cơ thể tôm sau 10 ngày phơi nhiễm là 7,85±1,03 μg/g. Mức độ này không khác biệt so với nhóm đối chứng (Hình 1 và Bảng 2 Kết quả này cho thấy tôm có khả năng điều hòa chì hiệu quả khi tiếp xúc với kim loại này đơn lẻ. Khả năng điều hòa này có thể được giải thích bởi các cơ chế bài tiết và ly giải lysosome trong gan tụy tôm. Nồng độ chì trong cơ thể tôm sau 10 ngày phơi nhiễm là 102,77±61,20 μg/g. Mức độ này cao hơn đáng kể so với nhóm đối chứng và nhóm điều trị đơn lẻ (Hình 1).Sự gia tăng nồng độ chì có thể do tác dụng hiệp đồng của các kim loại khác trong nước.Nghiên cứu trước đây đã chỉ ra rằng sự hiện diện của các kim loại khác có thể làm tăng khả năng hấp thu và tích lũy chì ở các sinh vật dưới nước. Tôm thẻ chân trắng có khả năng điều hòa chì trong cơ thể, nhưng khả năng này có thể bị ảnh hưởng bởi sự hiện diện của các kim loại khác.Cần có thêm nghiên cứu để hiểu rõ hơn về cơ chế tác động của hỗn hợp kim loại đối với sự tích lũy chì trong tôm thẻ chân trắng.
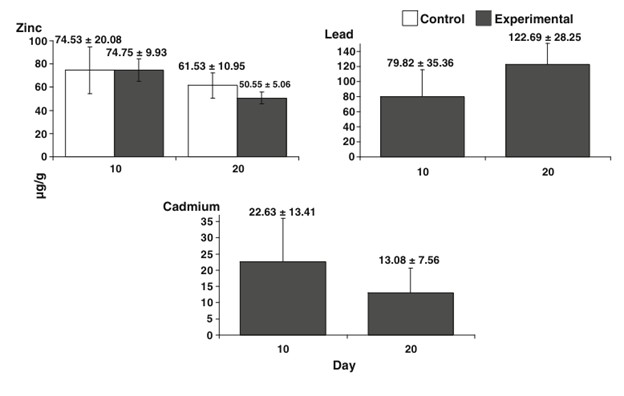
Thử nghiệm làm sạch cho thấy khả năng điều hòa chì của tôm thẻ chân trắng (P. vannamei) bị ảnh hưởng bởi sự hiện diện của các kim loại khác (như kẽm và cadmium). Sau 10 ngày phơi nhiễm với hỗn hợp kim loại, nồng độ chì trong cơ thể tôm không thay đổi đáng kể khi được chuyển sang môi trường nước sạch. Kết quả này cho thấy hỗn hợp kim loại có thể làm tổn hại đến khả năng điều hòa chì của tôm, dẫn đến sự tích lũy kim loại trong cơ thể. Nồng độ chì sau khi làm sạch vào ngày 10: 79,82 ± 35,56 μg/g, Ngày 20: 122,69 ± 28,25 μg/g (Hình 2). Sự khác biệt giữa ngày 10 và 20 do sự hiện diện của 2 mẫu có nồng độ chì thấp hơn (60 μg/g) trong ngày 10. So sánh nồng độ chì sau 10 ngày phơi nhiễm và sau 10 ngày làm sạch không có sự khác biệt đáng kể về mặt thống kê (p=0.07). Khả năng điều hòa chì của tôm bị tổn hại bởi sự hiện diện của các kim loại khác. Hỗn hợp kim loại có thể gây ra tổn thương tế bào ảnh hưởng đến các cơ chế điều hòa chì của tôm. Mokhtar và cộng sự quan sát thấy thiệt hại tương tự ở P. monodon khi tiếp xúc với niken và/hoặc cadmium.
Cadmium được phát hiện trong tất cả các nhóm được xử lý bằng Cd (>1,15 ng/g), với sự tích lũy rõ ràng được quan sát (Hình 1). Nồng độ trung bình trong cơ thể sau 10 ngày phơi nhiễm là 2,82± 0,67 μg/g ở dạng được xử lý bằng Cd và 17,42±3,09 μg/g ở dạng được xử lý bằng hỗn hợp kim loại (Cd-Mx). Sau 10 ngày làm sạch, nồng độ cadmi trong cơ thể tôm không thay đổi đáng kể (Bảng 3). Điều này cho thấy tôm thẻ chân trắng có khả năng bài tiết cadmi rất hạn chế. Khả năng tích lũy cadmi và bài tiết hạn chế đã được quan sát thấy ở các loài tôm khác, như P. indicus. Một số loài giáp xác khác cũng không thể bài tiết cadmi hiệu quả, ví dụ như amphipod Echinogammrus pirloti và các loài thuộc họ Balanus. Khả năng tích lũy cadmi của P. vannamei có thể được sử dụng để đánh giá mức độ ô nhiễm cadmi trong môi trường biển. Tôm thẻ chân trắng có thể được sử dụng như một sinh vật chỉ thị sinh học để theo dõi sức khỏe của hệ sinh thái biển.
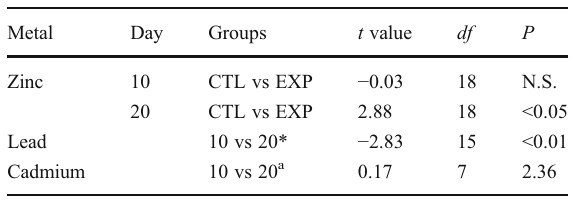
Tổng giá trị nồng độ trong cơ thể được báo cáo bằng µg/g (trung bình ± SD), sau 10 ngày phơi nhiễm (ngày 10) và 10 ngày để làm sạch (ngày 20)
N.S. không khác biệt đáng kể, nhóm thử nghiệm EXP
a Giá trị chỉ được so sánh giữa ngày 10 và ngày 20
Như đã trình bày ở trên, khi các con vật được xử lý bằng hỗn hợp kim loại, chúng đạt nồng độ trung bình là 17,42 μg/g, lớn hơn so với nhóm được xử lý riêng lẻ bằng cadmium (Hình 1 và Bảng 2), cho thấy lượng tiêu thụ cao hơn liên quan đến hỗn hợp. Mô hình này cho thấy mức độ nhạy cảm cao hơn của loài với sự kết hợp kim loại này.
Tôm thẻ chân trắng (Penaeus vannamei) có khả năng tự điều hòa nồng độ kẽm và chì trong cơ thể, giúp duy trì cân bằng kim loại ở mức an toàn. Tuy nhiên, khi tiếp xúc với hỗn hợp kim loại gồm kẽm, chì và cadmi, khả năng điều hòa này bị suy giảm đáng kể. Trong đó, cadmi không được kiểm soát hiệu quả và có xu hướng tích lũy trong mô tôm theo thời gian. Chính đặc điểm này khiến tôm thẻ chân trắng trở thành sinh vật chỉ thị sinh học tiềm năng trong việc giám sát mức độ ô nhiễm cadmi trong môi trường nước. Tuy nhiên, sự tương tác phức tạp giữa các kim loại trong hỗn hợp có thể ảnh hưởng đến cơ chế điều hòa tự nhiên của tôm, từ đó hạn chế khả năng sử dụng loài này để theo dõi các kim loại khác. Để hiểu rõ hơn cơ chế này, cần có thêm các nghiên cứu chuyên sâu ở cấp độ mô, tế bào và phân tử. Đặc biệt, nên tập trung vào các bề mặt trao đổi ion như mang, ruột và da – nơi diễn ra quá trình hấp thu và điều chỉnh kim loại, nhằm làm sáng tỏ các biến đổi sinh lý và sinh hóa trong điều kiện ô nhiễm kim loại hỗn hợp.
Theo Gabriel Núñez-Nogueira, Laura Fernández-Bringas, Alfredo Ordiano-Flores, Alejandro Gómez-Ponce, Claudia Ponce de León-Hill, Fernando González-Farías
Biên dịch: Nguyễn Thị Quyên – Bình Minh Capital
Xem thêm:
- Các Nghiên Cứu Mới Xác Nhận Tính Khả Thi Của Các Phương Pháp Cải Tiến Để Xử Lý Nước Thải Nuôi Trồng Thủy Sản
- Protein Loại Metallothionein Và Mức Dự Trữ Năng Lượng Sau Khi Tiếp Xúc Với Ni Và Pb Ở Tôm Thẻ Chân Trắng Penaeus vannamei
- Đánh Giá Thức Ăn Có Nguồn Gốc Từ Nannochloropsis Cho Cá Rô Phi

 English
English