Kỹ Thuật Nuôi, Tin tức
Phần 1: Vai trò của hormone tập trung sắc tố đỏ trong việc điều hòa hệ thống thần kinh nội tiết cuống mắt ở cua bùn Scylla paramamosain
Tóm tắt
Cuống mắt là cơ quan thần kinh nội tiết chiếm ưu thế ở giáp xác, tổng hợp họ hormone tăng đường huyết giáp xác (CHH) tham gia vào các hoạt động sinh lý như phát triển buồng trứng, cân bằng glucose và lột xác. Hormone tập trung sắc tố đỏ (RPCH) góp phần vào sự đa dạng của các ảnh hưởng sinh lý, bao gồm cả sự phát triển buồng trứng; tuy nhiên, vai trò của nó trong việc điều chỉnh các neuropeptide họ CHH trong cuống mắt vẫn chưa rõ ràng. Nghiên cứu này đã mô tả thụ thể RPCH (RPCHR) ở cua bùn Scylla paramamosain và phát hiện ra rằng nó được biểu hiện trong nhiều loại mô, bao gồm cả cuống mắt. Việc sử dụng peptide RPCH trưởng thành trong cơ thể sống đã hạn chế đáng kể biểu hiện hormone ức chế sinh noãn hoàng (VIH) và tăng cường đáng kể biểu hiện gen RPCHR, hormone tăng đường huyết giáp xác (CHH) và hormone ức chế lột xác (MIH), trong khi ngược lại, tiêm RPCH-dsRNA trong cơ thể sống để hạ gục đã làm tăng đáng kể biểu hiện VIH và làm giảm biểu hiện RPCHR, CHH và MIH trong cuống mắt. Nghiên cứu này báo cáo toàn diện rằng RPCH có thể điều chỉnh quá trình trưởng thành của buồng trứng, cân bằng glucose và lột xác ở S. paramamosain thông qua điều chế neuropeptide họ CHH trong cuống mắt.
1. Giới thiệu
Hormone tập trung sắc tố đỏ (RPCH), paralog của hormone giải phóng gonadotropin (GnRH) (Alexander và cộng sự, 2018), là một trong những hormone quan trọng nhất trong họ tác nhân sắc tố, kiểm soát những thay đổi về màu sắc của lớp biểu bì và chuyển động của các hạt sắc tố ở giáp xác, cũng như tăng độ nhạy cảm của võng mạc, nâng cao lượng đường trong máu, nhịp sinh học và thúc đẩy sự trưởng thành của tuyến sinh dục (Zeng và cộng sự, 2016; Alexander và cộng sự, 2018; Wei và cộng sự, 2021). Cho đến nay, hơn 50 loại peptide RPCH đã được phát hiện ở côn trùng và giáp xác, bao gồm cua bờ xanh Carcinus maenas, cua bùn cam Scylla olivacea, cua xanh Callinectes sapidus, tôm sú Penaeus monodon và tôm thẻ chân trắng Litopenaeus vannamei, và một số octapeptide được xác định ở nhiều loài giáp xác khác nhau có cùng trình tự (pQLNFSPGWamide), cho thấy cấu trúc được bảo tồn cao ở giáp xác (Martínez-Perez và cộng sự, 2005; Kornthong và cộng sự, 2013; Alexander và cộng sự, 2018). RPCH thuộc họ peptide hormone sinh mỡ (AKH)/RPCH và các protein tiền thân của nó đều mã hóa một peptide tín hiệu, một peptide liên kết với RPCH và một peptide trưởng thành RPCH (Glu-Leu-Asn-Phe-Ser-Pro-Gly-Trp) (Zeng và cộng sự, 2016; Martínez-Perez và cộng sự, 2005). RPCH chủ yếu được tổng hợp bởi phức hợp tuyến X-cơ quan xoang (XO-SG) trong hạch cuống mắt và phân bố rộng rãi ở các vùng chính của hệ thần kinh trung ương (CNS) giáp xác, bao gồm hạch bụng, hạch ngực và não, cũng như tủy ngoài, tủy trong và tủy tận cùng trong hạch cuống mắt (Zeng và cộng sự, 2016; Kornthong và cộng sự, 2013; Martínez-Perez và cộng sự, 2005), cho thấy rằng nó thực hiện nhiều chức năng. Ví dụ, RPCH làm tăng nồng độ glucose trong huyết tương của loài rận gỗ thô thông thường Porcellio scaber bằng cách huy động các kho dự trữ năng lượng (Zrala và cộng sự, 2010; Harlıoglu và cộng sự, 2020). Một hiện tượng tương tự cũng đã được xác định ở C. maenas, tức là RPCH có thể điều chỉnh tình trạng tăng đường huyết bằng cách liên kết với thụ thể RPCH (RPCHR) (Alexander và cộng sự, 2018). Việc sử dụng RPCH trong cơ thể sống có hiệu quả trong việc thúc đẩy quá trình trưởng thành giảm phân của trứng ở cua đồng Trung Quốc Eriocheir japonica (Wei và cộng sự, 2021). Ở tôm càng xanh Procambarus clarkii, RPCH hoạt động gián tiếp như một chất dẫn truyền thần kinh kích thích giải phóng hormone kích thích sinh dục (GSH) ở não và hạch ngực hoặc thúc đẩy sự phát triển của buồng trứng bằng cách đẩy nhanh quá trình tổng hợp methyl farnesoate (MF) ở cơ quan hàm dưới (Sarojini và cộng sự, 1995). Tiêm RPCH góp phần làm tăng đáng kể nồng độ hemolymph vitellogenin (Vg), biểu hiện Vg buồng trứng và đường kính tế bào trứng, dẫn đến tác động tích cực đến sự phát triển buồng trứng của L. vannamei (Chen và cộng sự, 2018). Tuy nhiên, tác động của RPCH trong cuống mắt giáp xác cần được nghiên cứu thêm.
Ở giáp xác, phức hợp XO–SG đóng vai trò là trung tâm điều hòa thần kinh – nội tiết thiết yếu, tương tự hệ thống dưới đồi – tuyến yên ở động vật có xương sống. Hệ thống này kiểm soát nhiều quá trình sinh lý quan trọng như sự phát triển buồng trứng, quá trình lột xác, điều hòa đường huyết và cân bằng thẩm thấu thông qua việc tổng hợp, lưu trữ và giải phóng một nhóm hormone tăng đường huyết ở giáp xác (CHH). Nhóm hormone này bao gồm hormone ức chế sinh noãn hoàng (VIH), hormone tăng đường huyết ở giáp xác (CHH), peptide vận chuyển ion (ITP), hormone ức chế cơ quan hàm dưới (MOIH) và hormone ức chế lột xác (MIH) (Liu và cộng sự, 2018; Chen và cộng sự, 2020). Bên cạnh đó, các chất dẫn truyền thần kinh và neuropeptide như 5-hydroxytryptamine, dopamine, allatostatin loại A (AST-A) và neuropeptide F ngắn (sNPF) tham gia điều hòa nhiều quá trình sinh lý thông qua việc tác động lên họ hormone CHH (Lorenzon và cộng sự, 2005; Wang và cộng sự, 2022, 2023). Tuy nhiên, vai trò đóng góp của RPCH đối với họ CHH tại hạch cuống mắt hiện vẫn còn hạn chế và cần được tiếp tục nghiên cứu làm rõ.
Cua bùn Scylla paramamosain chủ yếu phân bố ở các vùng nhiệt đới và ôn đới ấm của miền nam Trung Quốc và khu vực Ấn Độ Dương – Thái Bình Dương, là một trong những loài giáp xác quan trọng được đánh bắt và nuôi trồng kinh tế cho nghề cá xa bờ ở Trung Quốc và Đông Nam Á (Ye và cộng sự, 2011). Sản lượng hàng năm hiện tại đạt 154.661 tấn, đứng đầu Trung Quốc về sản lượng nuôi trồng giáp xác biển (Cục Thủy sản và Quản lý Nghề cá, 2023). Các neuropeptide họ CHH như VIH, MIH và CHH (ba dạng đồng phân: CHH1, CHH2 và CHH3) đã được đặc trưng từ cuống mắt S. paramamosain và tham gia vào quá trình điều hòa quá trình sinh noãn hoàng, lột xác và nồng độ glucose ở loài này (Liu và cộng sự, 2018, 2019; Huang và cộng sự, 2015). Với nhu cầu ngày càng tăng đối với S. paramamosain, việc cắt bỏ cuống mắt thường được thực hiện để làm bất hoạt VIH nhằm kích thích sự phát triển của buồng trứng (Liu và cộng sự, 2018). Tuy nhiên, các nhà nghiên cứu đang tìm kiếm các kỹ thuật thay thế để tránh một số hiện tượng sinh lý không mong muốn liên quan đến việc cắt bỏ cuống mắt, chẳng hạn như giảm khả năng nở và tỷ lệ đẻ trứng, tăng tỷ lệ chết (Liu và cộng sự, 2018). Ở S. paramamosain, sNPF-dsRNA, AST-dsRNA và microRNA (miR-277) đã được báo cáo là thúc đẩy quá trình hình thành noãn hoàng (Wang và cộng sự, 2023, 2022; Jia và cộng sự, 2021). Peptide RPCH trưởng thành trong S. paramamosain bao gồm 8 gốc axit amin, có trọng lượng phân tử thấp và dễ tổng hợp (Zeng và cộng sự, 2016), do đó có tiềm năng ứng dụng trong việc phát triển một kỹ thuật cắt bỏ cuống mắt thay thế. Để minh họa chức năng của RPCH trong họ CHH của cuống mắt S. paramamosain, trình tự thụ thể RPCH đã được nhân bản từ S. paramamosain và mô hình biểu hiện của nó đã được mô tả bằng cách sử dụng PCR phiên mã ngược (RT-PCR). Ngoài ra, chức năng điều hòa của RPCH trên các peptide họ CHH trong cuống mắt đã được nghiên cứu bằng cách làm im lặng RPCH bằng sự can thiệp của RNA sợi đôi (dsRNA). Nghiên cứu này cung cấp bằng chứng đầu tiên cho thấy RPCH có liên quan đến nhiều hoạt động nội tiết khác nhau ở S. paramamosain bằng cách điều hòa các neuropeptide họ CHH trong cuống mắt và thúc đẩy quá trình sinh noãn hoàng bằng cách ức chế biểu hiện VIH, dự kiến sẽ góp phần khai thác một kỹ thuật cắt bỏ cuống mắt thay thế ở giáp xác.
2. Vật liệu và phương pháp
2.1. Thu thập mẫu và thuốc thử hóa học
Cua S. paramamosain cái khỏe mạnh (42,37 ± 0,15 g) ở giai đoạn giữa quá trình lột xác được mua từ chợ thủy sản địa phương tại quận Haicang, thành phố Hạ Môn, tỉnh Phúc Kiến, Trung Quốc. Cua được thích nghi trong các bể riêng biệt chứa nước biển sục khí có độ mặn 29 ± 1 ppt và nhiệt độ 28 ± 0,5℃ trong một tuần trước khi tiến hành thí nghiệm. Trong quá trình thích nghi, ốc đồng tươi (Cipangopaludina chinensis) nặng khoảng 5% cua được cho ăn một lần một ngày và nước trong bể được thay mới một nửa ngày.
Một cysteine được thêm vào đầu carboxyl của amid hóa peptide trưởng thành RPCH (pGlu-Leu-Asn-Phe-Ser-Pro-Gly-Trp-NH2), được tổng hợp tại GL Biochem Ltd. (Thượng Hải, Trung Quốc), với độ tinh khiết là 99,87%.
2.2. Phân lập RNA và tổng hợp cDNA sợi đầu tiên
Tổng RNA được lấy từ cuống mắt, hạch não, hạch ngực, cơ quan hàm dưới, buồng trứng, cơ, tế bào máu, mang, biểu bì, gan tụy, dạ dày và ruột giữa bằng thuốc thử TRIzol (Invitrogen, Hoa Kỳ) theo hướng dẫn của nhà sản xuất. Nồng độ RNA được đo bằng máy quang phổ Q6000 (Quawell) và tính toàn vẹn được đánh giá bằng điện di gel agarose 1,5% (w/v). cDNA sợi đầu tiên được đặc trưng bằng PCR phiên mã ngược (RT-PCR) với bộ dụng cụ PrimeScript™ RT (TaKaRa) được trang bị gDNA Eraser.
2.3. Nhân bản phân tử, tin sinh học và phát sinh loài của RPCHR
Trình tự cDNA một phần của RPCHR được tạo ra từ bản sao mã của S. paramamosain và sau đó được xác nhận bằng cách thiết kế các đoạn mồi đặc hiệu. Tất cả các đoạn mồi được sử dụng trong nghiên cứu này đều được liệt kê trong Bảng 1. Trình tự ORF và amino acid (aa) được ước tính bằng phần mềm DNAMan, và trọng lượng phân tử và điểm đẳng điện lý thuyết (pI) được đánh giá bằng công cụ trực tuyến ExPASy-ProtParam (http://www.expasy.ch/cgi-bin/protparam). Các miền cấu trúc bảo tồn protein được dự đoán bằng công cụ phân tích trực tuyến NCBI Conserved Domains (http://www.ncbi.nlm.nih.gov/Structure/cdd/wrpsb.cgi). Các miền cấu trúc xuyên màng được dự đoán bằng công cụ TMHMM (https://services.healthtech.dtu.dk/services/TMHMM-2.0/) và căn chỉnh nhiều trình tự được thực hiện bằng ClustalX2.0 và GeneDoc. Cây phát sinh loài được thiết lập bằng phương pháp neighbor-joining với 1000 lần lặp bootstrap sử dụng phần mềm MEGA 7.0. Cấu trúc ba chiều (3D) được dự đoán bằng SWISS-MODEL và các miền cấu trúc protein được vẽ sơ đồ bằng phần mềm DOG_2.0.1.
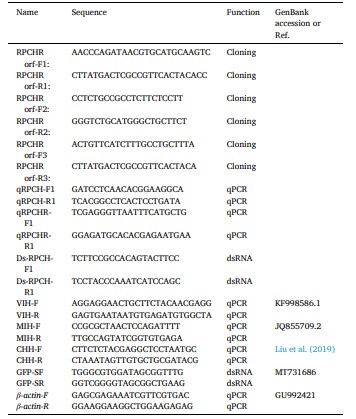
2.4. Phân bố mô của mRNA RPCHR
Mẫu biểu hiện của RPCHR trong 12 mô (hạch cuống mắt, hạch não, hạch ngực, cơ quan hàm dưới, buồng trứng, cơ, tế bào máu, mang, biểu bì, gan tụy, dạ dày và ruột giữa) đã được nghiên cứu bằng RT-PCR sử dụng RPCHR -F/R làm mồi. Đồng thời, β-actin được mở rộng với mồi β-actin-F/β-actin-R làm tham chiếu nội bộ. Sử dụng ddH2O làm đối chứng âm tính, tất cả các đoạn mồi được trình bày trong Bảng 1. PCR được thực hiện với DNA polymerase Ex-Taq® hiệu suất cao (Takara) như sau: biến tính trước 3 phút ở 95℃, 33 chu kỳ 95℃ trong 10 giây, 60℃ trong 35 giây và 72℃ trong 35 giây và khuếch đại thêm ở 72℃ trong 8 phút. Các phân đoạn PCR được tách trên gel agarose 1,0%, quan sát và chụp ảnh bằng máy chụp ảnh gel UV.
2.5. Tiêm peptide trưởng thành RPCH
40 con cua được tách nhanh thành hai nhóm ở giai đoạn tiền vitellogenic. Nhóm được điều trị bằng RPCH được dùng 10 ng/g trọng lượng cơ thể peptide trưởng thành tổng hợp bằng RPCH hòa tan trong dung dịch muối sinh lý giáp xác (CPS) (nồng độ cuối cùng trong huyết tương là ~ 5 × 10-6 mol/L), và nhóm đối chứng được truyền cùng một thể tích CPS. Nó được sử dụng làm đối chứng đo lường ban đầu cho bốn con cua chưa được điều trị. Tất cả các lần tiêm đều được thực hiện từ màng đáy của chân bơi. Các mẫu Cuống mắt được lấy từ bốn con cua tại các thời điểm cụ thể (0 giờ, 3 giờ, 6 giờ, 9 giờ, 12 giờ và 24 giờ) và được sử dụng để chuẩn bị RNA. Sau đó, các gen của họ neuropeptide CHH được định lượng bằng PCR định lượng thời gian thực (qRT-PCR) bằng cách sử dụng các đoạn mồi được liệt kê trong Bảng 1.
2.6. Tiêm RPCH dsRNA
Các đoạn mồi đặc hiệu RPCH dsRNA RPCH-dsRNA-F/R (Bảng 1) được hình thành bởi SnapDragon-dsRNA Design (https://www.flyrnai.org/cgi-bin/RNAi_find_primers.pl ), trong khi đó, gen protein huỳnh quang xanh (GFP) được dùng làm gen điều khiển ngoại sinh. Mục tiêu dsRNA được phiên mã bằng polymerase T7 và SP6 (Roche, Mannheim, Đức), sau đó tiêm RPCH dsRNA vào cua. S. paramamosain được chia ngẫu nhiên thành ba nhóm: tiêm RPCH dsRNA (5 μg/g; n = 5), tiêm GFP dsRNA (5 μg/g; đối chứng âm tính; n = 5) và tiêm CPS (kiểm soát dung môi; n = 5). Tất cả các lần tiêm đều được thực hiện từ màng đáy của chân bơi. Hai mũi tiêm được thực hiện cách nhau 24 giờ và Cuống mắt được lấy mẫu 48 giờ sau mũi tiêm đầu tiên. Các gen họ neuropeptide CHH trong Cuống mắt được định lượng bằng qRT-PCR.
2.7. qRT-PCR
Phân tích qRT-PCR được thực hiện trên hệ thống qPCR ABI 7500 sử dụng 2 × SYBR Select Master Mix (Applied Biosystems, Hoa Kỳ) và theo hướng dẫn của nhà sản xuất. Điều kiện chu kỳ qPCR: biến tính 94℃ trong 5 phút, sau đó là 40 chu kỳ: 94℃ (15 giây), 60℃ (30 giây), 72℃ (35 giây) (thu huỳnh quang) và cuối cùng là kéo dài ở 72℃ trong 10 phút. Tất cả các thí nghiệm được thực hiện trong ba bản sao kỹ thuật và các giá trị biểu hiện được chuẩn hóa với gen tham chiếu β-actin.
2.8. Phân tích thống kê
Dữ liệu qRT-PCR được tính toán bằng thuật toán 2−ΔΔCt và tất cả dữ liệu được biểu thị là giá trị trung bình ± SEM. Kiểm định tính chuẩn được thực hiện bằng cách sử dụng kiểm định Shapiro-Wilk với hiệu chỉnh Lilliefors và kiểm định tính đồng phương sai dựa trên kiểm định Levene. Sau đó, các khác biệt thống kê giữa các nhóm được phân tích bằng ANOVA một chiều (sau đó là kiểm định Duncan) hoặc kiểm định Student t-test (SPSS 16.0). Các khác biệt được coi là có ý nghĩa thống kê ở mức P < 0,05 và rất có ý nghĩa ở mức P < 0,01.
…Còn tiếp…
Theo Mei Wang, Jigui Yuan, Haihui Ye, Xiaohang Geng
Nguồn: https://www.sciencedirect.com/science/article/pii/S2352513424004836
Biên dịch: Nguyễn Thị Quyên – Bình Minh Capital
Xem thêm:
- Phân Tích Bệnh Phân Trắng (WFD) do Vibrio sp. Và Dinoflagellata Ở Tôm Thẻ Chân Trắng (Litopenaeus vannamei) Ở Ao Nuôi Nước Lợ
- Đâu Là Giải Pháp Thay Thế Khả Thi Cho Việc Cắt Bỏ Cuống Mắt Tôm?
- Ảnh Hưởng Của Việc Cho Ăn Trong Quá Trình Loại Bỏ Mùi Vị Khó Chịu Đến Sự Bài Tiết Geosmin Ở Cá Rô Phi

 English
English